|
|
|
|
|
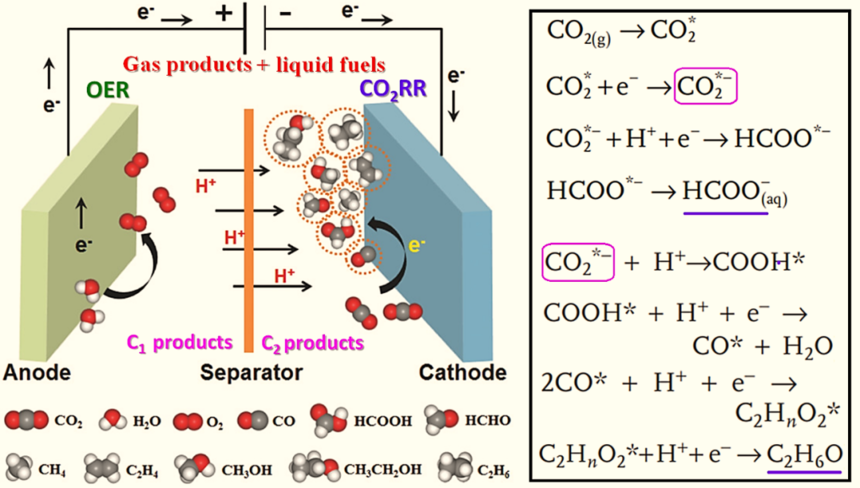
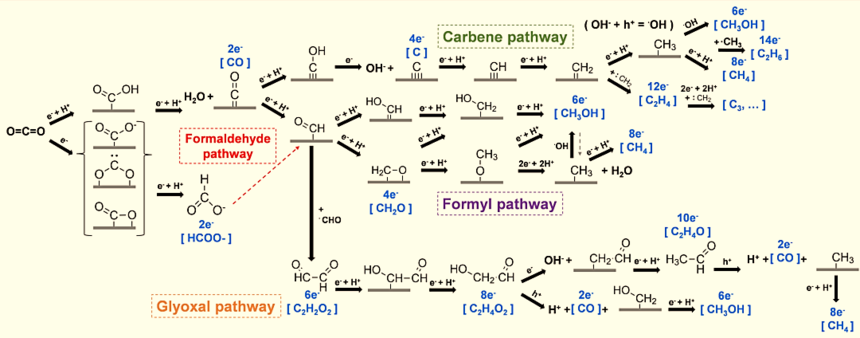
旋转圆盘电极装置用于二氧化碳还原反应CO2RR研究时间:2025-06-06 在全球气候变化日益严重的背景下,二氧化碳(CO2)作为主要温室气体的减少与转化问题成为了科学研究 的重要方向。二氧化碳还原反应(CO2RR)作为一种将CO2转化为有价值化学品的过程,不仅能够减轻温室气体 的排放,还具有潜在的经济价值。近年来,旋转圆盘电极(RDE)装置因其在电化学研究中的高效能与准确性, 受到了广泛关注。 旋转圆盘电极的设计与优化 为了提高RDE在CO2RR中的效率,研究者们进行了多方面的设计与优化。首先是电极材料的选择与改进。传统 的铂电极虽有良好的反应性,但由于其相对昂贵,许多研究者开始探索其它替代材料,例如铜、镍及其合金。铜电极 在CO2RR中表现出较好的选择性,能够选择性地还原为甲醇、乙烯等有价值的化学产品。 电极的结构设计也是提高反应效率的重要因素。一些研究者采用了纳米科技,对电极进行表面修饰,增加其比表 面积,增强对反应物的吸附能力,从而提升反应速率。例如,制备表面有微孔或纳米结构的电极,能够在较低的电压 下实现更高的还原效率。 RDE的旋转速度也会影响CO2的还原过程。通过优化旋转速度,研究者能够找到最佳的质量传输条件,以提高反 应物分子的传输速率和电极表面的反应速率。多项研究结果表明,适当的旋转速率不仅可以增强化学反应速率,还可 以提高反应的选择性。 二氧化碳还原反应(CO₂RR)之机理总结 虽然氢气(H2)是最佳的储能分子载体,但将二氧化碳(CO2)和水(H2O)转化为碳基燃料(例如CO、HCO OH和CH3CH2OH)的科学研究在最近一二十年来一直吸引着人们的兴趣。基于催化过程的二氧化碳还原反应(CO2RR) 最常见的包括电催化和光催化两大类别,具体的反应机制如下: (1)电催化CO2RR机制 对于电催化将CO2还原为甲酸(HCOOH)和/或乙醇(CH3CH2OH)液体燃料,其选择性(往往伴随着CO、CH4和C2H4 气体产物)和法拉第效率(可能伴随着严重的析氢竞争反应)仍难以满足实际生产要求(图1左)。与结晶材料相比,非晶材料通 常含有大量的低配位原子,因此存在大量的缺陷,进而产生更多的催化活性位点来提高电化学性能。例如,非晶态Cu催化 剂(a-Cu)具有较大的电化学活性面积和较强的CO2吸附能力,利用非晶态原子结构可促进CO2RR生成具有较高利用价值的 C1和C2液体燃料(图1右)[1]。 图1电催化CO2RR过程示意图和可能的产物。 电催化CO2RR制备多碳(C2+)液体燃料(例如乙醇(CH3CH2OH))具有挑战性,主要受限于反应中间体的稳定性及其后续 C-C偶联。最近,Hu等报道了一种独特的非晶态金属铜催化剂,即具有不饱和配位Cu位点的非晶CuTi合金(a-CuTi@Cu), 可用于电催化CO2还原生产多碳(C2~4)液体燃料[1]。理论计算和原位表征表明,非晶CuTi合金中亚表面Ti原子增加了表面 Cu位点的电子密度,增强了CO*的吸附,从而降低了CO*二聚或多聚所需的能垒。这种高效的电催化C-C偶联促进了多碳液 体燃料的生产,包括乙醇、丙酮和正丁醇,总C2~4-法拉第效率为49%。非晶态Cu基合金催化剂在CO2RR回收高附加值C2 +液体燃料和化学品方面具有良好的应用前景。 (2)光催化CO2RR机制 本文总结了光催化CO2转化制备C1和C2产物的可能反应机制,讨论了反应过程中关于表面物种吸附-脱附及质子-电子转 移的理论与实验的证据,指出了该领域面临的挑战,包括机理理解、反应器设计、经济效益,并提出了潜在的解决方案(图2)。 图2光催化CO2RR过程示意图和可能的产物。 在早期的综述中,Habisreutinger等人总结了从CO2在TiO2上形成五种C1(CO、HCOOH、CH2O、CH3OH、CH4)和 一些C2产物的三种可能机制,即甲醛途径(Formaldehydepathyway)、卡宾途径(Carbenepathway)和乙二醛途径 (Glyoxalpathway)。本文从文献中总结出了第四种路径,即甲酰路径(Formylpathway)。这些不同的可能性始于CO2在 催化剂表面的不同结合模式,包括氧配位、碳配位和侧向/混合配位。在此基础上,本文提出了一个全面的路径描述。途径是 由以下反应是否通过电子转移、质子转移(有时是羟基转移)或协同电子-质子转移发生来指示的。一个途径中的中间分子可 能是另一个途径的最终产物,如果它在进一步的步骤发生之前从催化剂的表面脱附。本文以不同得电子数的产物为顺序,逐 一分析总结了上述途径的特点和过程机理。 |